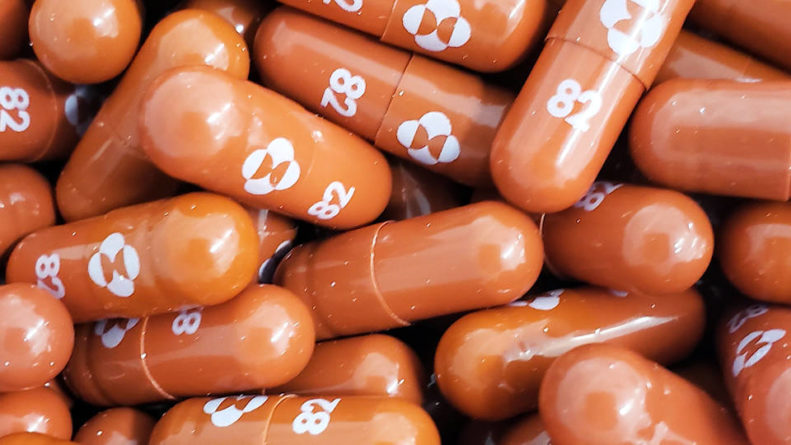
La compañía farmacéutica espera producir 10 millones de tratamientos con el comprimido molnupiravir para finales de 2021. De todas maneras, Merck asegura que este medicamento de vía oral no debe sustituir a la vacuna
El gigante farmacéutico estadounidense Merck informó el lunes (11.10.2021) que ha solicitado a las autoridades sanitarias de ese país la autorización de uso de emergencia de un medicamento de vía oral para tratar la enfermedad del Covid-19.
El comprimido se llama molnupiravir, «un medicamento antiviral oral en fase de investigación para el tratamiento del Covid-19 de leve a moderado en adultos que corren el riesgo de evolucionar a Covid-19 grave y/o de ser hospitalizados», dijo la empresa en un comunicado.
«Una urgencia sin precedentes»
La compañía dijo que estaba trabajando «con las agencias reguladoras de todo el mundo para presentar solicitudes de uso de emergencia o de autorización de comercialización en los próximos meses».
«El extraordinario impacto de esta pandemia exige que nos movamos con una urgencia sin precedentes», dijo Robert Davis, director ejecutivo y presidente de Merck.
Wendy Holman, directora ejecutiva de Ridgeback Biotherapeutics, socio de Merck, calificó la solicitud de «paso fundamental para poner el molnupiravir a disposición de las personas que pueden beneficiarse de un medicamento antiviral oral que puede tomarse en casa poco después del diagnóstico de Covid-19».
Un 50% de efectividad en la reducción del riesgo
Merck y Ridgeback llevaron a cabo un ensayo clínico entre unos 770 pacientes, de los cuales aproximadamente la mitad recibió un tratamiento de cinco días de la píldora, mientras que el resto, un placebo. Todos los pacientes tenían la enfermedad o mostraban síntomas.
De los que recibieron molnupiravir, el 7,3% fueron hospitalizados en el día 29, en comparación con el 14,1% de los que recibieron un placebo, lo que supone una reducción del riesgo relativo de alrededor del 50%.
El medicamento no debe sustituir a las vacunas
Las empresas afirmaron que la eficacia es la misma frente a todas las variantes, incluida la delta, y que el fármaco es seguro. Los expertos han dicho que no es una cura milagrosa y que debe complementar las vacunas, no sustituirlas.
Merck dijo en el comunicado que espera producir 10 millones de tratamientos para finales de 2021. Estados Unidos ya ha adquirido 1,7 millones de estos tratamientos de molnupiravir en caso de que se apruebe, con la opción de comprar más, mientras que la agencia de salud mundial Unitaid informó que estaba trabajando con una asociación llamada ACT-Accelerator para asegurar el suministro para los países de ingresos bajos y medios.